Cette équipe de l’Université de Washington Health Sciences fait une découverte remarquable : les effets du facteur de croissance des fibroblastes-1 (FGF1) sur certains types de cellules cérébrales spécifiques et sur les matrices extracellulaires appelées réseaux périneuronaux contribuent à expliquer comment « le cerveau » peut rétablir une glycémie normale chez des animaux diabétiques. C’est la découverte, documentée dans Nature Metabolism, de neurones glucorégulateurs et du rôle de ces structures à la fois dans le contrôle cérébral de l'homéostasie du glucose, et en tant que cibles prometteuses pour le traitement du diabète.
Les scientifiques montrent ici chez les rongeurs modèles de diabète de type 2, qu’une seule injection chirurgicale de la protéine FGF1 peut ramener la glycémie à la normale pendant des semaines ou des mois. Cependant, il restait à comprendre comment ce facteur de croissance agit dans le cerveau pour générer ce bénéfice durable. «Jusqu'à récemment, la capacité du cerveau à normaliser des taux élevés de sucre dans le sang d’animaux diabétiques n'était pas démontrée « , rappelle l’auteur principal, le Dr Michael Schwartz, professeur de médecine à l'Université de Washington.
Exploiter directement le potentiel inhérent du cerveau pour contrôler la glycémie
Comment FGF1 induit un contrôle glycémique cérébral : clarifier le processus sous-jacent pourrait permettre de développer de nouveaux traitements du diabète qui exploitent directement le potentiel inhérent du cerveau pour contrôler la maladie. « En interrogeant les réponses cellulaires et moléculaires induites dans l'hypothalamus par ce peptide cérébral FGF1, nous ouvrons la voie à une compréhension du processus mais aussi à de nouvelles stratégies thérapeutiques permettant d’obtenir une rémission durable du diabète ».
Vers un traitement plus durable ? Le diabète de type 2 affecte 10% de la population des pays riches. C’est une comorbidité étroite de l'obésité qi entraine des complications très sévères dont la maladie cardiaque, la perte de vision, une insuffisance rénale, la démence, des infections difficiles à guérir et des lésions nerveuses. Le contrôle de la glycémie peut prévenir ces problèmes, mais il est souvent difficile à atteindre et à maintenir sur la durée.
Ces travaux identifient à la fois :
- les cascades moléculaires en cause, de FGF1 et des voies de signalisation cérébrale, dans l’'hypothalamus et jusqu’au contrôle de la glycémie.
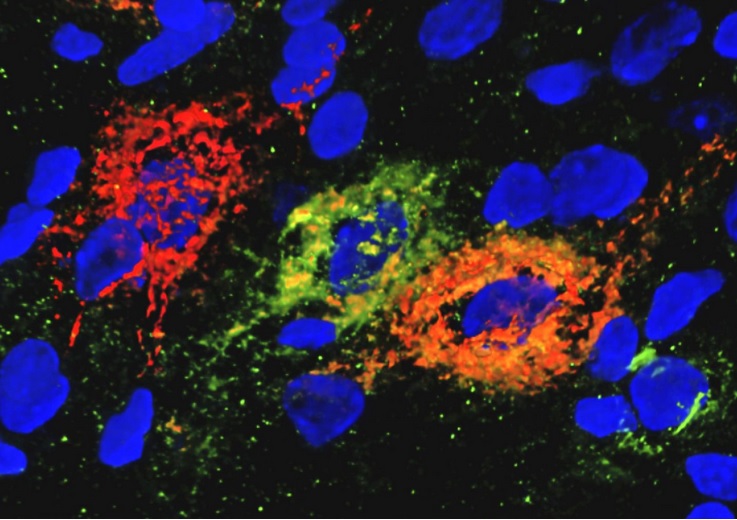
- D’autres études décryptent les assemblages de matrice extracellulaire appelés «réseaux périneuronaux» qui amalgament des groupes de neurones impliqués dans le contrôle de la glycémie (gluconeurones) ;
- le facteur de croissance des fibroblastes 1 répare ces réseaux périneuronaux endommagés par le diabète ;
- et cette réponse est nécessaire pour que la rémission du diabète soit durable.
- Les cellules gliales, qui non seulement fournissent un soutien structurel, mais aident également à organiser et à réguler l'activité de ces neurocircuits, répondent plus intensément que les neurones, au FGF1 ;
- des interactions améliorées sont également constatées entre les astrocytes et un sous-ensemble de neurones qui fabriquent des protéines liées à l'agouti (appelées neurones Agrp). Les neurones Agrp étant des composants essentiels du système de signalisation de la mélanocortine, un circuit cérébral essentiel au contrôle de l'alimentation, du poids corporel et de la glycémie. L’atténuation de la signalisation de la mélanocortine a été liée au développement du diabète chez les humains et les rongeurs ;
- enfin, parmi les autres types de cellules ayant répondu de manière robuste au facteur de croissance des fibroblastes-1, on trouve les tanycytes, des cellules gliales allongées, sensibles aux nutriments, trouvées uniquement dans l'hypothalamus. Leurs contributions à la normalisation des taux de glucose nécessitent une étude supplémentaire ;
- les réseaux périneuronaux regroupent les neurones régulateurs de la glycémie dans l'hypothalamus, y compris les neurones Agrp. La perte de filets périneuronaux est rapidement inversée après une seule injection de FGF1 dans le cerveau.
Ces découvertes soutiennent les réseaux périneuronaux comme des cibles clés pour la rémission soutenue du diabète induite par l'action du peptide FGF1. Les chercheurs pensent que ces réseaux ou matrices contribuent peut-être à limiter l'activité des neurones Agrp et à augmenter la signalisation de la mélanocortine.
Bref, de nouvelles stratégies en vue, ciblant ces réseaux périneuronaux, pour obtenir une rémission durable du diabète chez les patients.
Source : Nature Metabolism 07 September 2020 DOI : 10.1038/s42255-020-00275-6 Hypothalamic perineuronal net assembly is required for sustained diabetes remission induced by fibroblast growth factor 1 in rats
Plus sur Diabète Blog





